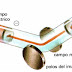
Supongamos que vertemos ácido clorhídrico en un matraz erlen-meyer que contiene virutas de cinc. Decimos que el contenido del matraz es un sistema químico. Observamos que este sistema sufre un cambio en sus propiedades a medida que transcurre el tiempo (todo o parte del cinc desaparece y se desprende un gas). El cambio de propiedades que experimenta un sistema químico es una transformación química o reacción química, y se representa mediante una ecuación química. La ecuación de nuestra reacción es:
En una mezcla o en una disolución, las sustancias químicas puestas en contacto permanecen inalteradas y la masa de la mezcla es igual a la suma de las masas de las sustancias componentes. Ahora bien, en el transcurso de una reacción química, algunas de las sustancias puestas en contacto desaparecen al mismo tiempo que aparecen otras nuevas. ¿Pero qué ocurre con la masa?
La aplicación sistemática de la balanza al estudio de las transformaciones químicas dio lugar al descubrimiento de las leyes de las reacciones químicas y al establecimiento de la química como ciencia.
Ley de conservación de la materia o Ley de Lavoisier
Hasta el siglo XVIII se piensa que una transformación química puede transcurrir con pérdida o ganancia de masa.
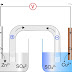
Esta idea permanece hasta que Antoine Lavoisier realiza una serie de experimentos, como la calcinación de estaño en un recipiente cerrado y comprueba que el peso total del recipiente no ha variado con la calcinación, que el metal se ha transformado en su óxido y ha aumentado de peso, que el peso del aire contenido en el recipiente ha disminuido y que el aumento de peso del metal es igual a la disminución del peso del aire.
A raíz de ésta y otras experiencias, Lavoisier, en 1789, enuncia la ley que lleva su nombre:
 |
| Padre de la Química. Creador de la Ley de Conservación de la Masa |
La masa de un sistema permanece invariable cualquiera que sea la transformación que ocurra dentro de él.
La ley de conservación de la materia no es absolutamente exacta, ya que con la teoría de la relatividad de Einstein:  los conceptos de materia y energía están interrelacionados. De acuerdo con la ecuación anterior, la materia puede desaparecer liberándose una gran cantidad de energía. Sin embargo, salvo en las reacciones nucleares, no tendremos en cuenta la relación materia-energía. En una reacción química ordinaria, en la que se pongan en juego 418 kJ (100 kcal), la masa disminuye en 4,65*10-12 kg, cantidad prácticamente despreciable.
los conceptos de materia y energía están interrelacionados. De acuerdo con la ecuación anterior, la materia puede desaparecer liberándose una gran cantidad de energía. Sin embargo, salvo en las reacciones nucleares, no tendremos en cuenta la relación materia-energía. En una reacción química ordinaria, en la que se pongan en juego 418 kJ (100 kcal), la masa disminuye en 4,65*10-12 kg, cantidad prácticamente despreciable.
En la próxima parte hablaremos de la Ley de las proporciones definidas o Ley de Proust